La Dra. Lucero Díaz Peralta es Investigadora posdoctoral en el Instituto de Ciencias Físicas de la Universidad Nacional Autónoma de México.
El Dr. Iván Martínez Duncker es Profesor Investigador del Centro de Investigación en Dinámica Celular, de la Universidad Autónoma del Estado de Morelos (UAEMor).
La Dra. Margarita I. Bernal Uruchurtu es Profesora Investigadora del Centro de Investigaciones Químicas de la UAEMor y es integrante de la Academia de Ciencias de Morelos.
Esta publicación fue revisada por el comité editorial de la Academia de Ciencias de Morelos.
La química
Sin duda alguna existen muchas formas de romper récords, de lograr proezas irrepetibles o reunir condiciones únicas. La química es una de las disciplinas científicas que ha sido catalogada dentro de un famoso libro de récords mundiales. La razón de ello es que cada año los especialistas de esta disciplina crean más de un millón de moléculas que un año antes no existían. La capacidad de generar nuevas sustancias químicas parecería ser inagotable. Sin embargo, eso no necesariamente es algo que el público en general considere como una gran hazaña. Recordamos que la hermanita menor de un compañero solía decir que la química era muy fácil, todo lo que tienes que hacer es poner A con B y entonces ya tienes el compuesto C. ¡Ojalá fuera tan sencillo! decimos todos los que hemos intentado obtener una de esos millones de moléculas novedosas. Lo cierto es que no hay “recetas” infalibles ni fórmulas mágicas para obtener una molécula que tenga un conjunto de características específicas. Los químicos dedicados a la síntesis de nuevos compuestos pueden corroborarlo. Justamente por esta razón, el trío formado por Carolyn R. Bertozzi, Morten P. Meldal y K. Barry Sharpless fueron elegidos por su importante contribución a la química como merecedores del Premio Nobel 2022. Y es que, en efecto, fueron premiados por descubrir una forma muy ingeniosa para construir muchos tipos de moléculas en condiciones muy favorables y aún en entornos químicamente muy complicados.

La investigadora Carolyn R. Bertozzi y los investigadores Morten P. Meldal y K. Barry Sharpless, ganadores del Premio Nobel de química 2022.
https://www.nobelprize.org/, https://www.bbc.com/mundo/noticias-63147363
Imaginemos que cada molécula es como una pieza del juego de armar LEGO®, hay desde piezas pequeñas con un solo conector hasta piezas con geometrías complicadas y con muchos conectores. Haciendo un símil con la química, cada uno de esos conectores es una posibilidad de formar una unión con otra pieza, un enlace químico. El enlace puede ser entre piezas iguales o piezas diferentes. Pensemos en el caso más simple posible: si tenemos dos tipos de piezas, las A y las B, puede suceder que dos piezas iguales se unan y tengamos A-A y B-B, pero, también puede ser que tengamos la combinación A-B y la B-A con lo que el resultado no es únicamente un producto, digamos C, sino cuatro combinaciones diferentes que seguramente tendrán propiedades distintas. Si uno está interesado en solamente uno de esos compuestos, digamos el A-B, tendrá que encontrar una forma de separarlo de sus hermanos químicos.
Entonces, el sueño de los químicos sintéticos es encontrar de qué forma cada vez que pongamos A y B en contacto, sólo obtengamos A-B.
La Química Clic: La conexión LEGO para el descubrimiento y aplicación de nuevas moléculas
La Academia Sueca señaló que los ganadores del Premio Nobel de Química 2022 se hicieron merecedores a éste por el desarrollo de la “Química Clic", la cual permite conectar moléculas como bloques de construcción, rápida y eficientemente, así, ¡en un clic! (Figura 1).
La especificidad y funcionalidad de las reacciones clic es un factor clave que las hace útiles en la investigación y las aplicaciones biomédicas por la forma en la que funciona. En 2001, Kolb, Finn y Sharpless definieron el término de “Química Clic” como la unión de dos bloques de construcción molecular de manera fácil, selectiva y con un alto rendimiento, en condiciones suaves, tolerantes al agua y con muy poca formación de subproductos. Entre las principales ventajas se encuentra el rápido acceso a nuevas familias de materiales interesantes y el fácil montaje de bibliotecas de moléculas pequeñas.
Sus aplicaciones se encuentran cada vez más en todos los aspectos del descubrimiento de fármacos, que van desde la búsqueda de pistas hasta la química combinatoria con la creación de enormes bibliotecas de compuestos, la química in
situ con una síntesis que se lleva a cabo en el lugar y momento adecuado y la proteómica con la investigación del ADN mediante reacciones de bio-conjugación particularmente en el desarrollo de nuevas moléculas para el tratamiento del cáncer.
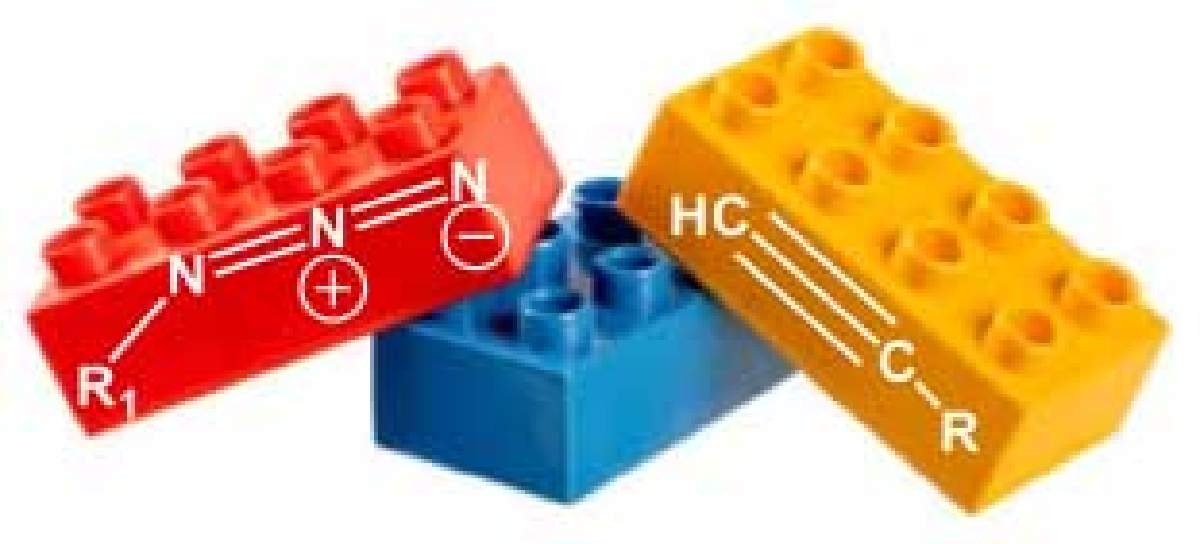
Figura 1. Unión de dos moléculas a través de la cicloadición alquino-azida (imagen tomada de: How Click Chemistry is Like Playing with LEGOs by William Ford Beimers).
Reacciones de cicloadición 1,3-dipolar
En los juguetes de armar hay grandes favoritos, los autos, los trenes o los barcos. En química, ese modelo favorito son las reacciones de cicloadición. Éstas resultan en la formación de un compuesto cíclico a partir de dos moléculas que reaccionan entre sí; un ejemplo muy importante de una reacción de cicloadición en el desarrollo de fármacos, son las cicloadiciones 1,3-dipolares.
Una de las reacciones de cicloadición 1,3-dipolar más conocida es la que se da entre un azida orgánico y un alquino. Un ejemplo de este tipo de moléculas (o piezas) aparece en la Figura 2. Este proceso, descubierto por Huisgen en 1963, forma un nuevo compuesto cíclico a partir de dos componentes, un compuesto dipolar (azida) 1 y un compuesto que contiene un triple enlace (alquino) 2. Los compuestos cíclicos resultantes son los triazoles 3 o 4 (Esquema 1). De hecho, los productos obtenidos pueden ser toda una familia de triazoles, en la que los grupos R1 y R2 ocupan las posiciones 1,4 del ciclo en 3 o bien como en 4, las posiciones 1,5.
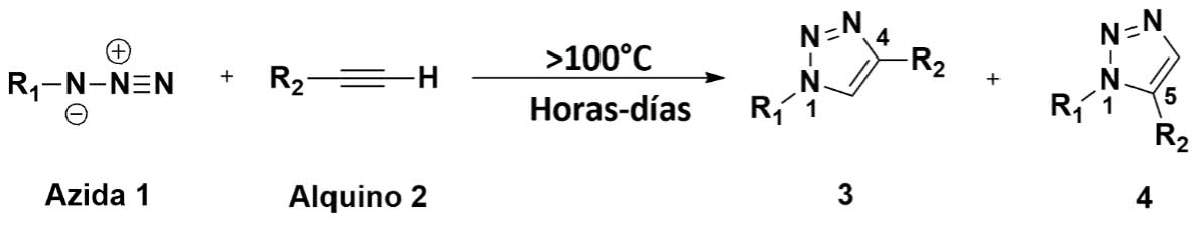
Figura 2. Reacción de cicloadición 1,3-dipolar
La reacción original de Huisgen requiere de tiempos prolongados de reacción y temperaturas elevadas, por lo que tuvo una aplicación muy limitada y por mucho tiempo permaneció poco estudiada. Sin embargo, a partir del año 2001, el uso de catalizadores metálicos, particularmente de cobre, revolucionó la reacción original de Huisgen, lo que dio lugar a lo que hoy conocemos como la cicloadición azida-alquino catalizada por cobre (CuAAC por sus siglas en inglés), procesos que hoy conocemos como la “Química Clic”.
Cicloadición azida-alquino catalizada por cobre (CuAAC)
Hay que tener en cuenta que Sharpless había ya sido reconocido con un premio Nobel en 2001 por sus estudios para obtener moléculas quirales ópticamente puras, uno de los retos más difíciles que enfrenta un químico sintético. Es decir, el mundo ya sabía que Sharpless era alguien con un enorme interés por encontrar recetas útiles y confiables para preparar moléculas con geometrías especiales. En muchas pláticas, seminarios y artículos había ya explicado la importancia de desarrollar un catálogo (recetario) para preparar bloques de construcción que funcionara siempre con excelentes resultados, tanto para obtener una pequeña cantidad de un compuesto, como en aplicaciones a gran escala.
En el año 2002, el grupo de Meldal en Dinamarca y el de Fokin y Sharpless en EUA descubrieron, de manera independiente, la habilidad de las sales de cobre (I) para acelerar las reacciones de cicloadición 1,3-dipolar, al punto en que éstas puedan llevarse a cabo a temperatura ambiente y formando exclusivamente el compuesto 3, lo que resulta en un mínimo trabajo de purificación.
La cicloadición azida-alquino catalizada por cobre (CuAAC) es una reacción que satisface todos los criterios establecidos por Sharpless para el concepto de “Química Clic” ya que esta reacción es simple de realizar, tiene altos rendimientos, y es muy selectiva para la formación del triazol 3. Utiliza precursores, los alquinos y los azidas, fácilmente disponibles y como catalizadores sales de Cu (I), con la enorme ventaja económica y ambiental de poder llevarse a cabo en disolventes no tóxicos, con mucha frecuencia agua, a temperatura ambiente y con sólo esperar algunos minutos (ver Figura 3). Estas modificaciones en la forma de hacer reacciones son muy importantes si lo pensamos en términos de la industria que debe sintetizar los fármacos. Acercar procesos de “Química Verde” conduce a una sostenibilidad ineludible en el tiempo actual.
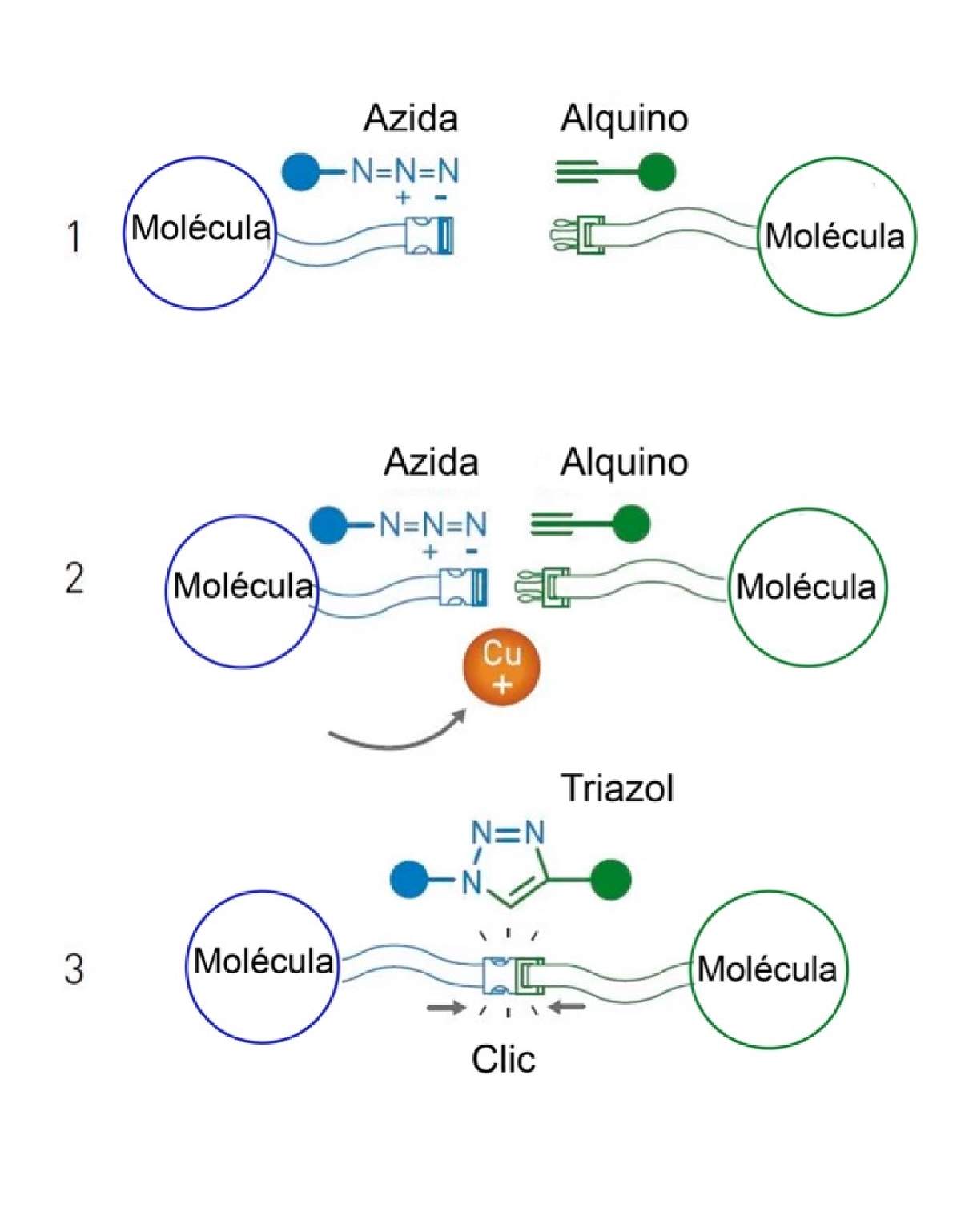
Figura 3. La Química Clic (Tomada de: https://www.nobelprize.org/prizes/chemistry/2022/popular-information/)
Aplicaciones farmacéuticas de la “Química Clic”
La visión de algunos y el trabajo de pensar en nuevas moléculas pronto abrió los ojos de muchos ante el poder de este pequeño truco sintético. La “Química Clic” ha resultado en la simplificación de la síntesis de compuestos, lo que acelera los procesos de descubrimiento de potenciales fármacos. Los productos de estas reacciones, particularmente los 1,2,3-triazoles, son estructuras que exhiben un amplio espectro de propiedades biológicas: su biocompatibilidad, es decir la habilidad de generar una respuesta positiva en un ambiente biológico, estrechamente relacionado con la química bioortogonal, su estabilidad a la degradación metabólica por hidrólisis ácida o básica y la formación de enlaces de hidrógeno con otras moléculas biológicas hacen que estos heterociclos se les considere “privilegiados” en química farmacéutica. Esto ha detonado el desarrollo de algunos fármacos que contienen este anillo entre las moléculas con propiedades anticancerígenas, antibacteriales y antivirales (Figura 4).
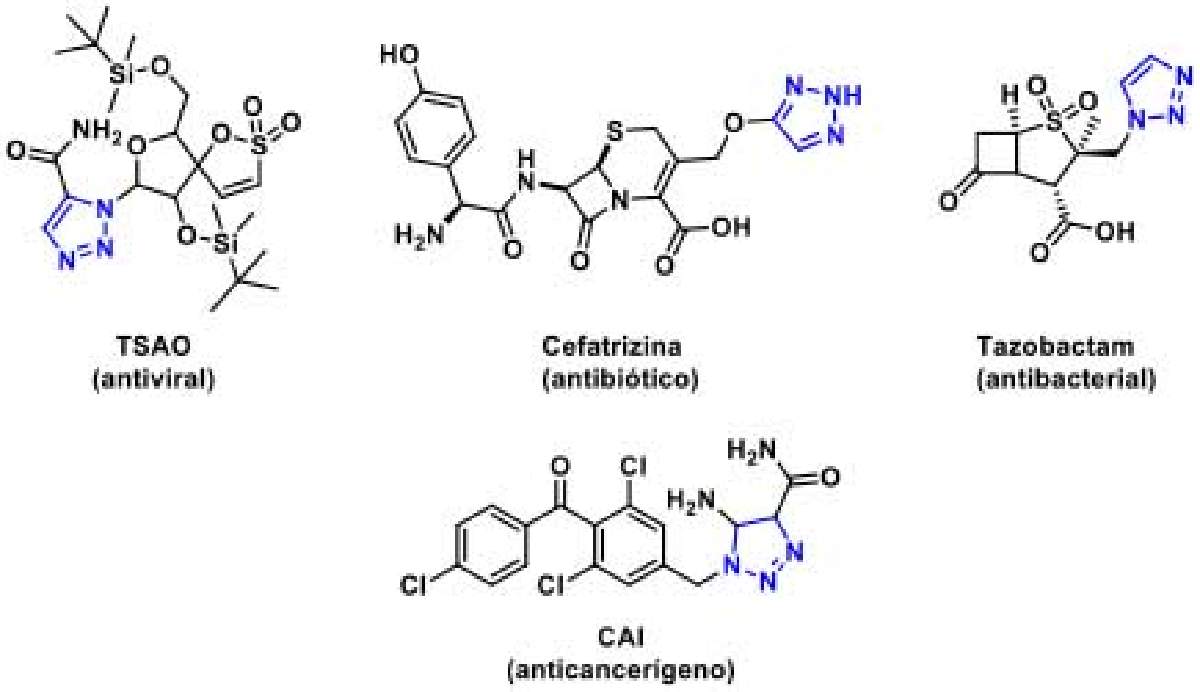
Figura 4. Fármacos comercialmente disponibles conteniendo 1,2,3-triazoles.
La pasión por los juegos de armar
Cuando Bertozzi estaba realizando su licenciatura en Química se dio cuenta que la síntesis de nuevos compuestos orgánicos le encantaba y decidió explorar la posibilidad de especializarse en ello. Sin embargo, los grupos de investigación a los que se acercó preguntando si podría entrenarse con ellos le respondieron, sistemáticamente, que no recibían mujeres en su equipo para evitar distracciones. Imaginen que en la década de los 80’s del siglo pasado esa era una respuesta que una talentosa joven mujer podía recibir de profesores universitarios y quizá pocos la consideraban una actitud discriminatoria. Afortunadamente, ella no se dio por vencida y se trasladó del Este de EEUU hacia California, en donde un joven profesor la aceptó en su grupo para estudiar la química sintética de azúcares. Querido lector, la dulce y relativamente pequeña molécula de azúcar que conoces en su forma de sacarosa o de glucosa C6H12O6, encierra las complicaciones y problemas más amargos de la química. Cada átomo de carbono está unido a un átomo de hidrógeno de un lado y, del otro, a un grupo OH. Hasta allí todo va bien, pero, si vemos el acomodo en el espacio veremos que el lado del que se encuentren los -OH puede determinar isómeros diferentes y, por tanto, propiedades distintas. Es decir, cada átomo de carbono es un centro asimétrico. Y no para allí, las moléculas pueden ser lineales o bien, cerrarse en forma de ciclos de cinco o de seis lados. Estos ciclos no son planos, son flexibles y pueden unirse entre sí para formar cadenas. Y sí, fueron estos “dulces” compuestos los que Bertozzi eligió de área de estudio para graduarse como química orgánica sintética.
Y, como si el reto de la química de los glúcidos (azúcares) no fuese suficiente, ella llevó a su equipo a trabajar en condiciones distintas a las que hasta ahora usaban los químicos sintéticos. En vez de hacer sus experimentos en condiciones controladas en un matraz en el que sólo están las moléculas que nos interesa unir y ninguna otra, con atmósfera controlada para que ni el aire las afecte, ella decidió probar estas reacciones en una sopa bioquímica, es decir en células. En un medio lleno de otras piezas que, potencialmente, pueden interferir con la reacción. Así, emprendió el enorme reto de innovar la aplicación de la química orgánica de los azúcares en el estudio de los sistemas vivos, con un profundo interés de hacerlo en el contexto del cáncer y el sistema inmune.
Llevando la Química Clic al interior de las células.
El estudio de los azúcares se centró por muchos años en su aspecto metabólico como proveedores de energía para sustentar la función de nuestras células. Sin embargo, su función se ha ampliado a la de codificar información biológica. Nuestras células, así como las de todos los seres vivos, construyen una gran variedad de estructuras formadas por azúcares: los glicanos. Los glicanos se encuentran dentro de las células, en su superficie e incluso en el entorno que les da soporte (matriz extracelular). Si imaginamos la vista aérea de un bosque, bien podría ser la misma perspectiva la que tendríamos si sobrevoláramos la superficie celular, donde los árboles serían los glicanos. Así de abundantes son, es decir, están muy lejos de ser simples elementos decorativos. Por ejemplo, más de la mitad de todas las proteínas en nuestro cuerpo se encuentran glicosiladas, es decir, unidas a glicanos, sin los cuales no funcionarían.
¿Por qué su abundancia? Bueno, los glicanos son moléculas que las células utilizan para transmitir información biológica, codifican un lenguaje biológico que está expresado en su forma más visible sobre la superficie celular, justo el punto ideal que una célula tiene para comunicarse con su entorno. Este lenguaje es reconocido por proteínas que lo “leen” y desencadenan los procesos de comunicación celular indispensables para organizar la interacción entre nuestras células y de éstas con su entorno. Entre estos procesos se incluye su interacción con distintos patógenos como el virus SARS-CoV-2, el cual tiene una proteína en su superficie con abundantes glicanos que, entre otras cosas, le permite escapar de la respuesta inmune.
Los glicanos en sus diversas formas son sintetizados en el interior de la célula, específicamente en el aparato de Golgi y el retículo endoplásmico, mediante un proceso mediado por la acción de enzimas conocidas como glicosiltransferasas. Las glicosiltransferasas utilizan distintos azúcares (en el ser humano hay nueve diferentes tipos que pueden utilizar) para sintetizar glicanos, a través de un proceso ordenado y secuencial, así como una línea ensambladora de autos. Este proceso de sintetizar glicanos y unirlos a otras macromoléculas (proteínas, lípidos o ARN) se conoce como glicosilación.
Los glicanos son los biopolímeros más diversos y estructuralmente complejos, encontrándose generalmente unidos a proteínas y lípidos. Recientemente, Ryan Flynn, de la Universidad de Harvard, quien se formó en el grupo de Bertozzi, descubrió mediante el uso de la “Química Clic”, que los glicanos también se encuentran asociados al ácido ribonucleico o ARN, el cual participa en la síntesis de las proteínas y realiza la función de mensajero de la información genética.
Debido a su complejidad y a diferencia de las proteínas o los ácidos nucleicos que pueden ser manipulados fácilmente, el estudio de los glicanos y su función biológica se mantuvo en rezago respecto a otras macromoléculas biológicas, ya que los investigadores no tenían las herramientas específicas para estudiarlos. Además de las complicaciones que tiene la química de glicanos, imaginemos la complicación adicional en un contexto donde los glicanos celulares pueden cambiar en cuestión de minutos. En 1996, cuando Bertozzi inició su trabajo en la Universidad de Berkeley, ella y sus estudiantes desarrollaron métodos para estudiar la estructura y el funcionamiento de los azúcares en las células. Más o menos en ese tiempo empezó a pensar si sería posible hacer reacciones de química orgánica en el interior de células u organismos vivos sin matarlos (química in vivo).
Su trabajo la llevó a diseñar nuevas reacciones que eventualmente le conduciría a aprovechar las capacidades de la “Química Clic” para visualizar la dinámica de los glicanos en la superficie de las células. Bertozzi ideó suministrar a las células, azúcares modificados que fueran incorporados en la síntesis de los glicanos, pero sin que la modificación interfiriese con el proceso normal de la glicosilación. Es decir, que las glicosiltransferasas responsables de sintetizar los glicanos no se “percataran” de la diferencia entre el azúcar normal y el azúcar modificado. Esa es justamente la característica de la química bioortogonal, realizar transformaciones químicas entre reactivos no biológicos (abióticos) en sistemas vivos y sin interferencias. Es decir, que la reacción química bioortogonal no afecte procesos bioquímicos propios de la célula, ni que los procesos bioquímicos de la célula afecten la reacción bioortogonal. ¿Qué modificación en los azúcares podría pasar inadvertida por las glicosiltransferasas que sintetizan los glicanos? Bueno, la modificación debía consistir en un pequeño cambio químico en el azúcar que añadiera un grupo funcional que serviría de “asa química”, la cual posteriormente, mediante la reacción con otra molécula, permitiría identificar al azúcar modificado, una vez que éste ya formara parte de los glicanos en la superficie de la célula. Se decidió por introducir un grupo azida como el asa química ideal, desarrollando nuevas estrategias químicas para poder conjugar otras moléculas a esta asa química una vez que el monosacárido modificado se encontraba formando parte de un glicano en la superficie celular. Cuando se estaba dando a conocer la Química Clic CuAAC desarrollada por los grupos de Medal y Sharpless, Bertozzi reconoció que esta química podría aplicarse a los azúcares con grupos azida que había estado utilizando. Desafortunadamente, la dependencia del cobre de estas reacciones conllevaba a la toxicidad de este elemento para las células y organismos en los que ella quería estudiar la glicosilación. Inspirada en trabajos de Georg Wittig y Adolf Krebs de los años 60 del siglo pasado, desarrolló finalmente en el 2004 una “Química Clic sin cobre” conocida como cicloadición azida-alquino promovida por tensión anular.
Mediante esta “Química Clic Bioortogonal”, Bertozzi emprendió el reto de visualizar la dinámica biológica del ácido siálico, un monosacárido que forma parte de los glicanos humanos y que tiene una gran importancia biológica, incluyendo el cáncer. Para ello, sintetizó azúcares precursores del ácido siálico que contenían grupos azida. Estos precursores fueron suministrados a células, ratones y embriones de peces cebra. Así el ácido siálico-azida que se producía dentro de la célula se incorporó a los glicanos, pudiendo ser detectado por la “Química Clic sin cobre”, al poder unirle moléculas fluorescentes que tenían grupos alquino o ciclooctinos conjugados con péptidos FLAG, permitiéndole “ver” a los glicanos en la superficie celular, mediante diversas técnicas incluyendo la microscopía. Este proceso de detección, libre de toxicidad y que se podía llevar a cabo con una rapidez de unos cuantos minutos, permitió observar la composición de los glicanos celulares y sus cambios dinámicos a lo largo de la vida de una célula.
Así la Química Clic Bioortogonal, tuvo su entrada estrepitosa en el estudio de los seres vivos, en un primer momento, en el estudio de los glicanos mediante la síntesis de otros azúcares modificados con azida. Después, a lo largo ya de casi 20 años, se extendió al estudio de muchas otras moléculas biológicas y en escenarios biológicos muy distintos. Esto ha conducido a la posibilidad de generar reacciones clic bioortogonales en el interior de tumores y así liberar fármacos antitumorales que solo en el interior del tumor se activan, logrando incrementar su concentración en ese sitio y disminuyendo su toxicidad en el resto del cuerpo.
Esta gran diversidad de reacciones químicas útiles son en parte la consecuencia de haber generado grupos de investigación diversos. En las palabras de Bertozzi, la diversidad de ideas es útil para encontrar estrategias novedosas y una forma de promover la diversidad es asegurar que los grupos de trabajo tengan personas de diferentes grupos sociales, con diferentes gustos, preferencias e historias. Quizá, el reto de ser mujer y además ser abiertamente gay en un medio en el que solo los hombres hacían la mayor parte de la investigación en síntesis orgánica, la movió a la aventura sintética y enfrentar con su genio los retos sociales y científicos que la vida le puso enfrente, llegando incluso a ser una reconocida activista por la diversidad en la ciencia. La astucia de ella fue iluminada por saber que la inteligencia no tiene ni prejuicios, ni nichos privilegiados en dónde alojarse. Todos están invitados a la aventura del conocimiento.
Para saber más:
Sobre catalizadores e isómeros moleculares:
Sobre los ganadores
Esta columna se prepara y edita semana con semana, en conjunto con investigadores morelenses convencidos del valor del conocimiento científico para el desarrollo social y económico de Morelos. Desde la Academia de Ciencias de Morelos externamos nuestra preocupación por el vacío que genera la extinción de la Secretaría de Innovación, Ciencia y Tecnología dentro del ecosistema de innovación estatal que se debilita sin la participación del Gobierno del Estado.


