Marco A. Morales es Licenciado en Bioquímica Diagnóstica egresado de la Facultad de Estudios Superiores Cuautitlán, UNAM. Actualmente es estudiante de maestría en el programa de Ciencias Bioquímicas en el Instituto de Biotecnología de la UNAM. Anteriormente realizó su tesis de licenciatura en LANGEBIO en el laboratorio de Evolución de la Diversidad Metabólica. Cuenta con estancias de investigación en el laboratorio de Diagnóstico Molecular del Hospital Regional 1° de Octubre del ISSSTE y como becario del programa MITACS International en Queen’s University en Kingston, Canadá.
Adelfo Escalante es Doctor en Biotecnología por la Facultad de Química, UNAM. Investigador Titular del Departamento de Ingeniería Celular y Biocatálisis del Instituto de Biotecnología, UNAM. Miembro del Sistema Nacional de Investigadores Nivel II. Presidente de la Sociedad Mexicana de Biotecnología y Bioingeniería, A. C. para el período 2018-2020. Sus líneas de investigación se enfocan en la ingeniería de vías metabólicas en las bacterias Escherichia coli y Pseudomonas chlororaphis, enfocado a la producción de compuestos aromáticos.
Esta publicación fue revisada por el comité editorial de la Academia de Ciencias de Morelos.
Cuando pensamos en bacterias es muy común que lo primero que venga a nuestra mente sean enfermedades y suciedad. Sin embargo, por mucho tiempo, la ciencia ha estudiado a estos microorganismos y ha ampliado la idea que tenemos acerca de ellos. Además de la gran importancia que tienen en el equilibrio de los ecosistemas, las bacterias han sido utilizadas en un sin fin de desarrollos biotecnológicos. Estos avances nos permiten mejorar nuestra calidad de vida, empleando a las bacterias en diferentes procesos y obteniendo de ellas una gran cantidad de moléculas de gran importancia médica, alimentaria, incluso tecnológica e industrial.
Dentro de estas moléculas, existe un grupo de compuestos químicos conocidos como fenazinas. Estos compuestos son producidos principalmente por bacterias que habitan mares y suelos, generalmente en la rizosfera, que es la zona del suelo cercana a las raíces de las plantas.
Estas moléculas tienen una estructura química muy particular y se ha demostrado que tienen un papel muy importante en la supervivencia de las bacterias que las producen y en cómo se relacionan con su entorno. Sin embargo, son las diferentes aplicaciones que podemos darles lo que ha despertado un gran interés científico e industrial.
¿Qué son las fenazinas?
En términos completamente técnicos y estructurales las fenazinas se definen como un grupo de compuestos químicos que se conocen como metabolitos secundarios y cuya estructura molecular central siempre es un anillo de pirazina (1,4-diazabenceno) que presenta dos bencenos anulados, la cual puede tener diferentes grupos funcionales unidos haciendo la diferencia entre una fenazina y otra (para mayor información sobre los detalles de la estructura de las fenazinas puede consultar la referencia de Blankenfeldt, 2013). Pero dejémoslo en algo más sencillo: son moléculas de estructura compleja y muy variable producidas por algunas bacterias, principalmente pertenecientes al género Pseudomonas y Streptomyces (Figura 1).
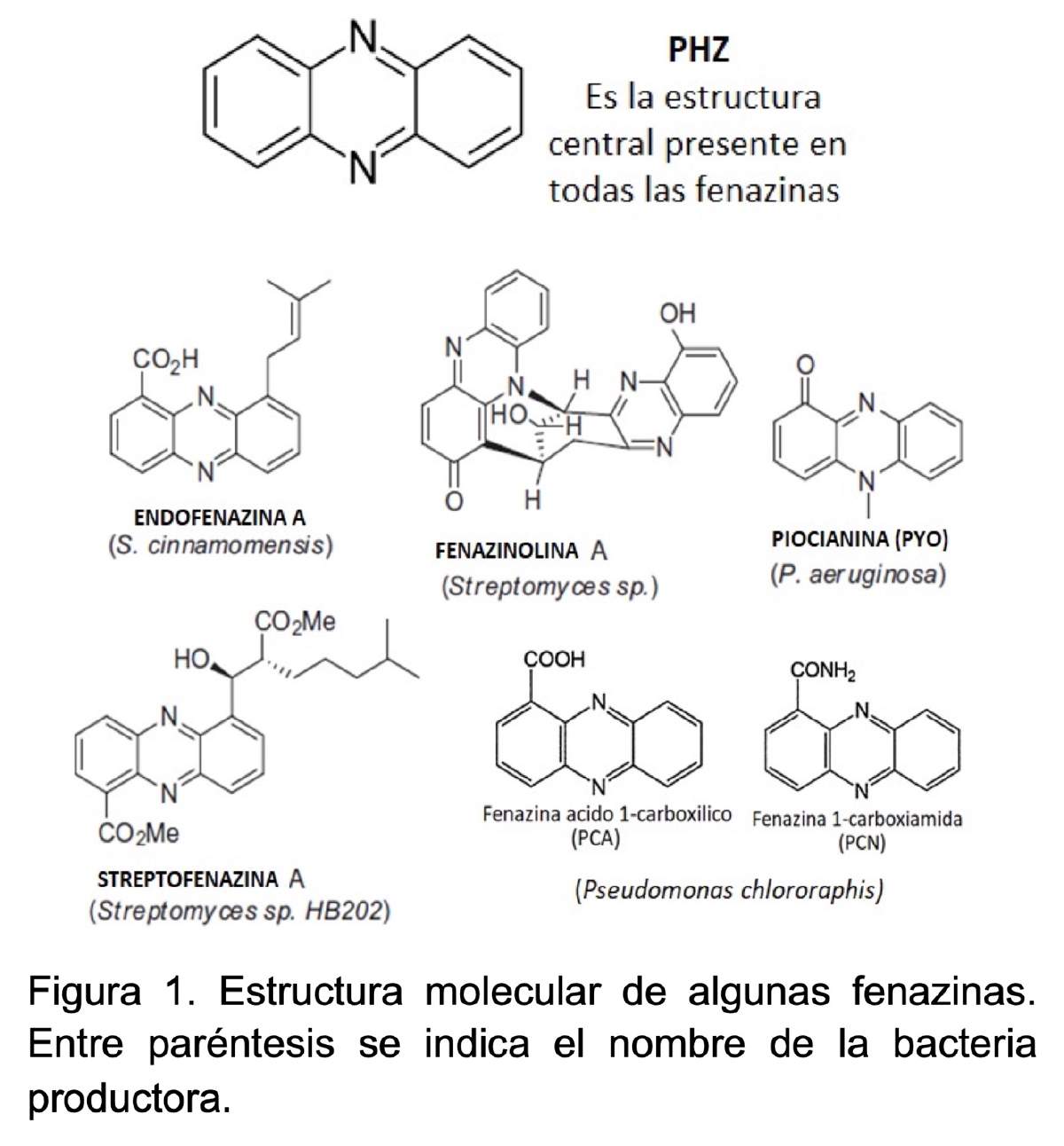
La estructura compleja de las fenazinas les brinda la característica de tener un alto potencial redox, es decir, pueden perder y ganar electrones de manera fácil, lo cuál las convierte en moléculas altamente reactivas y con el potencial de liberar energía química que puede ser transformada en energía eléctrica. Una peculiaridad distintiva de estos compuestos es su color. Hay fenazinas con coloración amarilla, roja, naranja, verde, azul e incluso morada. Estos colores son más fáciles de apreciar cuando las bacterias que las producen crecen en medios de cultivo en el laboratorio. Matraces y cajas Petri con vivos y alegres colores abundan en los laboratorios que estudian estos compuestos. Por si no fueran ya lo suficientemente llamativas, estas moléculas son también fluorescentes, es decir, bajo luz ultravioleta emiten un brillo radiante (Figura 2).
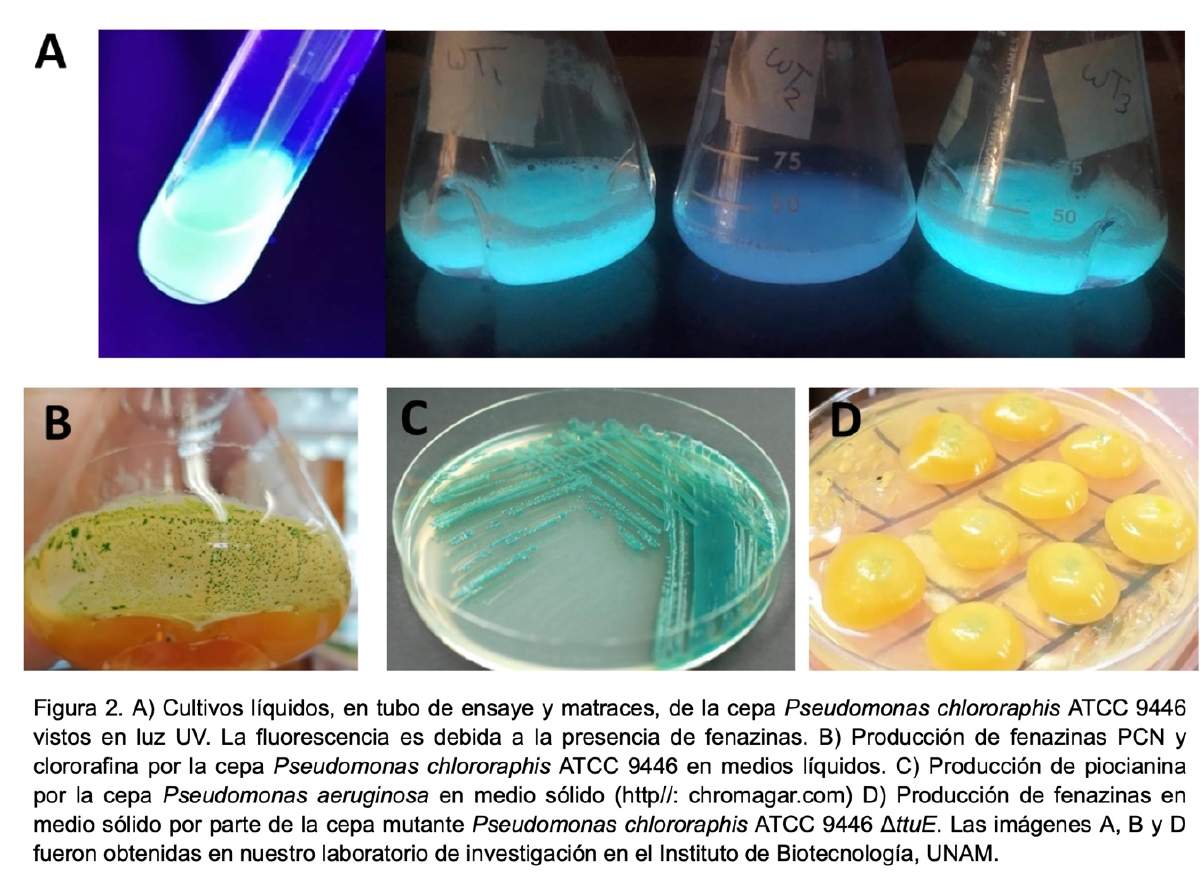
Resulta interesante la manera en que las fenazinas fueron descubiertas. Aunque hemos mencionado que las fenazinas son principalmente producidas por bacterias que habitan nichos silvestres, hay una especie bacteriana productora de estos compuestos llamada Pseudomonas aeruginosa que puede infectar las heridas de pacientes con el sistema inmune debilitado. Las heridas infectadas por esta bacteria se caracterizan por liberar un pus de un color verde azulado. Pues bien, fue a partir de muestras de este pus que en 1859 Mathurin-Joseph Fordos, un fotógrafo francés aisló la primer fenazina: la piocianina, y es justo esta molécula de coloración verde azulado, la causante de la peculiar apariencia del mencionado pus. A partir de ese momento y hasta la fecha se han descubierto más de 180 fenazinas y sintetizado más de 6000 tipos.
La ventaja de producir fenazinas en la naturaleza
Como mencionamos, las fenazinas se consideran un metabolito secundario. Los metabolitos son compuestos que producimos todos los seres vivos a través de las reacciones bioquímicas que ocurren en nuestras células: a partir de un sustrato, como puede ser una fuente de carbono la célula sintetiza estas moléculas y energía necesarias para vivir. En el caso de las bacterias el metabolismo se ha dividido en dos tipos para facilitar su estudio: metabolismo primario y metabolismo secundario. De manera muy sencilla, el metabolismo primario les sirve a las bacterias para crecer y multiplicarse y así incrementar su población en un determinado ambiente, mientras que el metabolismo secundario les sirve para generar moléculas que están asociadas a procesos de adaptación, supervivencia e interacciones ecológicas, siendo los antibióticos, uno de los ejemplos mas conocidos.
Como metabolitos secundarios, las fenazinas les confieren muchas ventajas a las bacterias que las producen. Por una parte, les sirven para defenderse y competir con otros microorganismos, pues las fenazinas funcionan como antibióticos (inhiben el crecimiento de bacterias) y antifúngicos (inhiben el crecimiento de hongos). De igual manera, las fenazinas al ser compuestos altamente reactivos pueden alterar las características fisicoquímicas del ambiente en el que viven las bacterias que las producen, de tal manera que reprimen o favorecen el crecimiento de otras especies microbianas que habitan en el mismo ambiente. Se ha demostrado también, que las bacterias productoras de fenazinas que causan infecciones en humanos y animales, utilizan a estas moléculas para evadir al sistema inmune y generar mayor daño en los tejidos que invaden.
Además de brindarles protección y ventaja en su entorno, las fenazinas les permiten a las bacterias del suelo que las producen generar una relación simbiótica con las plantas, es decir, una relación donde ambas partes se beneficien. Por una parte, las propiedades antibióticas y antifúngicas de las fenazinas evitan que las raíces de las plantas sean infectadas por diversos microorganismos fitopatógenos, e incluso les brindan protección contra algunos insectos y nematodos (gusanos redondos o cilíndricos). Al mismo tiempo, el crecimiento de las bacterias productoras de fenazinas en las raíces de las plantas promueven la producción de exudados en las raíces aportando nutrientes que promueven el crecimiento de estas bacterias y continuar con la producción de fenazinas, cerrando así este ciclo de ayuda mutua. Se ha determinado también que las fenazinas denominadas como PCA (fenazina ácido carboxílico), PCN (fenazina carboxi amida) promueven los mecanismos de defensa de las plantas.
Otro aspecto importante de mencionar es la relación que se ha descrito entre la producción de fenazinas y formación de biopelículas o biofilms en las raíces de las plantas que colonizan las bacterias Pseudomonas chlororaphis. El biofilm es una estructura compleja, producida por bacterias y está conformada principalmente por proteínas, polisacáridos y ADN. Este biofilm funciona como una matriz, una película viscosa, donde se pueden adherir otras bacterias, de una o varias especies, y formar un microbioma. Se ha demostrado que la producción de fenazinas promueve la formación de un biofilm, permitiéndole a las bacterias adherirse de una mejor forma a las raíces de la planta que colonizan y crear un entorno más seguro para protegerse de diferentes amenazas, como la alteración del pH, alteración de la osmolaridad y escasez de nutrientes. La producción de biofilms en las raíces de la planta promueve también un nivel de hidratación elevado promoviendo protección a la raíz contra desecación y se ha propuesto el desarrollo de “suelos sanos” por agregación de partículas de suelo en los biofilms (para más información sobre la interacción entre Pseudomonas con plantas y la producción de fenazinas y biofilms consultar la referencia de Anderson y Kim, 2020).
Aplicaciones Biotecnológicas de las fenazinas
Hemos descrito algunas de las principales actividades biológicas que tienen las fenazinas, las cuales le otorgan ventajas importantes a las bacterias que las producen en la naturaleza. Sin embargo, gran parte del interés científico en estos compuestos radica en las aplicaciones biotecnológicas que les podemos dar a estas moléculas. Hasta el momento, la principal aplicación para las fenazinas se ha dado en la agricultura, pues han sido utilizadas para el control de plagas e infestaciones por hongos y bacterias. Para esto se pueden emplear soluciones de fenazinas o se puede aplicar en los plantíos, preparados directamente a partir del medio de cultivo de las bacterias productoras. La ventaja de utilizar fenazinas con estos fines es que tienen un impacto ambiental mucho más bajo que los plaguicidas químicos tradicionales y representan un menor riesgo para la salud humana pues no se acumulan en los alimentos cosechados y tienen baja toxicidad.
En los últimos años también se ha investigado la aplicación médica que pueden tener las fenazinas. La más importante es su uso como nuevos antibióticos, pues cada vez es más común que muchos de estos compuestos pierden eficacia para erradicar algunas infecciones y que las dosis deban aumentarse o cambiar los esquemas de antibióticos por otros más potentes. Esto puede llegar a generar resistencias a estos compuestos, lo cual es un gran problema de salud pública a nivel global. Las nuevas moléculas generadas a partir de la estructura central de las fenazinas han demostrado ser potentes antibióticos. Un ejemplo son compuestos halogenados derivados de fenazinas, algunos de los cuales han demostrado ser antibióticos bastante potentes, requiriendo concentraciones muy bajas (0.03 µM) para inhibir a la bacteria patógena común Staphylococcus aureus, lo cual es bastante menor a la concentración requerida de otros antibióticos ya conocidos, como la vancomicina, que tiene el mismo efecto inhibitorio, pero a una concentración de (1.38 µM equivalente a 2 miligramos por litro). Estos nuevos antibióticos aún se encuentran en estudios para determinar a qué dosis son seguros para consumo humano y sus posibles efectos secundarios, para posteriormente pasar a una fase de estudios clínicos y poder ser aprobado su uso terapéutico. Otra aplicación que se ha explorado para las fenazinas es su propiedad como agentes anticancerígenos. Esto debido a que se han identificado fenazinas que interfieren con las actividades de las enzimas topoisomerasa I y II, las cuales son enzimas que se ha demostrado son muy activas en células cancerosas. En la actualidad son varios compuestos sintetizados a partir de fenazinas los que ya se encuentran en pruebas de fase clínica para su uso terapéutico, como el compuesto TBI-1004 que es derivado de benzo fenazinas para combatir infecciones causadas por cepas de Mycobacterium tuberculosis resistentes a antibióticos, o el fármaco XR11576, que es un derivado de aril fenazinas con actividad anticancerígena.
Otro de las aplicaciones más innovadoras de las fenazinas es en el desarrollo de nuevos sistemas bioelectroquímicos. Estos sistemas, incluyendo su variante más importante que es la Pila de Combustible Microbiana (PCM), se están desarrollando rápidamente, siendo tecnologías prometedoras para la producción de energía renovable y el tratamiento de aguas residuales, entre otras aplicaciones. La tecnología de PCM tiene como objetivo generar corriente eléctrica a través de la transferencia extracelular de electrones, que los microorganismos liberan de sustratos orgánicos, como las fenazinas, las cuales, al tener un alto potencial redox, es decir pueden perder o ganar electrones con facilidad, son moléculas idóneas para este tipo de tecnología.
Mejorando la producción de fenazinas
Como hemos visto, las fenazinas son moléculas muy interesantes y con un gran potencial de aplicaciones, es debido a esto que muchos grupos de investigación alrededor del mundo enfocan sus esfuerzos en entender mejor la biología que hay detrás de estas moléculas, desarrollar procesos que mejoren y aumenten su producción, métodos para modificarlas y obtener nuevos compuestos y todas las aplicaciones que estos desarrollos puedan tener.
Las fenazinas se han producido en laboratorio desde la década de los 1970s, y la manera más sencilla de hacerlo es creciendo bacterias productoras de estas moléculas en medios de cultivo muy ricos a cierta temperatura y condiciones de oxigenación dependiendo de la especie bacteriana. Sin embargo, una limitante a superar es el poco rendimiento que se obtiene de estos compuestos, pues por lo general se obtienen miligramos, o incluso microgramos de fenazinas por litro de cultivo. En la actualidad, son dos las principales estrategias que se exploran para abordar esta problemática, no solo con las fenazinas si no, en general, con cualquier molécula de interés producida en cultivos microbianos.
La primera es mejorar las condiciones de cultivo, es decir realizar modificaciones a la temperatura, oxigenación, agitación o al medio de cultivo empleado. Las variaciones al medio de cultivo pueden ser cambiar la formulación (agregando o disminuyendo la cantidad de algún nutriente en específico) cambiar el tipo de medio (sólido o líquido) o incluso agregar algún compuesto que genere algún estrés al cuál respondan las bacterias produciendo nuestro compuesto de interés (por ejemplo, se ha visto que agregando algún compuesto que genere estrés oxidativo o componentes de membrana de hongos al medio de cultivo puede incrementar la producción de fenazinas).
La segunda estrategia consiste en emplear a la ingeniería genética de diversas formas. Se pueden realizar modificaciones genéticas directamente al microorganismo productor del compuesto de interés para agregar o quitar genes, o realizar mutaciones en genes específicos; estas modificaciones se hacen con el objetivo de que en el metabolismo de la bacteria se priorice la producción del compuesto de interés. Otra manera es lo que se conoce como expresión heteróloga, y consiste en tomar a los genes que codifican a las enzimas involucradas en la producción de nuestro compuesto de interés y transferirlos a algún otro microorganismo modelo donde la producción sea mejor. Por lo regular la bacteria Escherichia coli, que crece rápidamente en medios de cultivo baratos y para la cual ya hay una gran cantidad de herramientas genéticas disponibles para favorecer la expresión de genes ajenos.
En nuestro laboratorio, en el Instituto de Biotecnología de la UNAM, estamos empleando ambas estrategias para incrementar la producción de fenazinas con la cepa bacteriana Pseudomonas chlororaphis ATCC9446. En específico esta cepa produce tres fenazinas: PCA, PCN y clororafina. Las primeras dos son de una coloración amarilla y la última se aprecia en forma de cristales verdes en cultivos bacterianos.
La primera estrategia que implementamos fue modificar la forma de cultivar a la bacteria. En lugar de mantener nuestro cultivo bacteriano líquido en agitación por 120 horas dentro de una incubadora, como por lo regular se hace, los dejamos en agitación solo 24 horas y el resto del tiempo en reposo. Esta modificación generó un estrés en las bacterias, pues al no haber agitación se limita la entrada de oxígeno en el medio, lo cual orilla a la bacteria a producir más fenazinas, pues estas moléculas pueden sustituir al oxígeno en un proceso bioquímico esencial llamado cadena respiratoria. Además, modificamos la formulación del medio de cultivo empleado; sustituimos glicerol, que es el carbohidrato más empleado para el cultivo del género Pseudomonas, por glucosa. El resultado fue de hasta siete veces más la producción de fenazinas.
Otra estrategia que estamos implementando es la eliminación de dos genes: uno que codifica para una enzima que regula de manera negativa la producción de fenazinas y otro que codifica una enzima que desvía el metabolismo hacia otras rutas metabólicas que no son la de las fenazinas.
Estos trabajos aún están en desarrollo y esperamos pronto obtener resultados concluyentes para que nuestros esfuerzos, junto con el de muchos otros científicos alrededor del mundo, permitan que en un futuro próximo podamos obtener un mayor provecho a estas moléculas tan interesantes, y que las fenazinas se incorporen a más procesos biotecnológicos de alta escala con bajo impacto ecológico que permitan la obtención productos que nos beneficien en temas de salud y cuidado al medio ambiente.
REFERENCIAS
Blankenfeldt W. (2013) Chapter 1 The Biosynthesis of Phenazines. Microbial Phenazines. Biosynthesis, Agriculture and Health. Springer. Washington.
Anderson J, et. al. (2018). Safety of Pseudomonas chlororaphis as a gene source for genetically modified crops. Transgenic Research. 2018; 27(1): 103–113.
Anderson A. and Kim Y. (2020). Insights into plant-beneficial traits of probiotic Pseudomonas chlororaphis isolates. Journal of Medical Microbiology 2020; 69:361–37.
Guttenberger N, Blankenfeldt W, Breinbauer R. (2017). Recent developments in the isolation, biological function, biosynthesis, and synthesis of phenazine natural products. Bioorganic & Medicinal Chemistry 25 (2017) 6149–6166.
Yue S, Bilal M, Song C. et. al. (2018). Development of an efficient method for separation and purification of trans-2,3-dihydro-3-hydroxyanthranilic acid from Pseudomonas chlororaphis GP72 fermentation broth. Separation and Purification Technology. 202 (2018) 144–148.
Esta columna se prepara y edita semana con semana, en conjunto con investigadores morelenses convencidos del valor del conocimiento científico para el desarrollo social y económico de Morelos. Desde la Academia de Ciencias de Morelos externamos nuestra preocupación por el vacío que genera la extinción de la Secretaría de Innovación, Ciencia y Tecnología dentro del ecosistema de innovación estatal que se debilita sin la participación del Gobierno del Estado.




